

科研动态

近日😂,国际权威期刊Journal of the American Chemical Society(JACS)在线发表了杏宇平台生命科学技术学院/杏宇平台注册瞿旭东团队与生命科学技术学院罗树坤团队的合作成果“A Stereoselective Decarboxylative Aromatase/Cyclase Directs the Biosynthesis of an Axially Chiral Biphenyl Framework in Fasamycin”。瞿旭东教授、罗树坤特别研究员为论文的共同通讯作者,博士生姜凯和博士生朱诚为本文的共同第一作者。
芳香聚酮是一大类具有多种生物活性的天然产物🚵🏽♀️。它们的生物合成主要由II型聚酮合成酶(PKSs)负责,其中minimal PKS组装聚酮链,随后由芳构化酶/环化酶(ARO/CYC)进行芳构化/环化反应🫅🏿,形成基本的芳香骨架🫰🏽。这些骨架作为模板,经过进一步的PKS后修饰,赋予芳香聚酮复杂的结构多样性。然而,尽管存在多种后修饰🍐,基本芳香骨架仅鉴定出八种不同的平面共轭结构(图1)。因此,发现能够催化新型环化模式的ARO/CYC,对于扩展芳香聚酮的结构多样性和功能多样性至关重要💆🏽♀️。
Fasamycin(FAS)及其同系物是一类芳香聚酮,因其对耐甲氧西林金黄色葡萄球菌(MRSA)和耐万古霉素屎肠球菌(VRE)的高效活性而备受关注。与典型的平面芳香骨架不同🥺,FAS 具有独特的轴手性联苯骨架(图1),表明其生物合成涉及一种新型的立体选择性 ARO/CYC 及一种特殊的生物合成机制。近期课题组已阐明 FAS 中phenyldimethylanthrone(PDA)核心的形成,该核心通过 TcmI 类 ARO/CYC(FasL)催化的四环环化反应生成👨👩👧👧,同时受一个非必需辅助 ARO/CYC(FasD)的影响((Proc. Natl. Acad. Sci. USA 2024, 121, e2321722121⛓️💥,图 2)🙇🏼♀️。然而🧚🏼♂️,轴手性联苯结构(即 E 环)的形成机制仍不清楚。

图 1. II 型芳香聚酮的基本芳香骨架。FAS具有显著区别于其他类型的轴手性骨架。
在本项研究中,联合课题组首先在体外重构了ABX和FAS途径中共享的PDA骨架的生物合成途径。进一步优化体外酶反应体系的pH和温度,并结合13C同位素标记🕵🏻♂️,发现从未鉴定的生物合成中间体 1才是FasU的真正底物🏃🏻♀️🆔。体外实验和体内回补证实,单加氧酶家族蛋白 FasU,其作为一类全新的芳香化酶/环化酶(ARO/CYC)📊,以严格的 S-立体专一性催化中间体 1依次进行脱羧和环化/芳构化反应👩🏿⚖️,负责FAS中轴手性联苯骨架的形成𓀕。为了深入理解ARO/CYC独特的脱羧/芳构化/环化/立体选择性机制🦔,联合课题组又解析了FasU的晶体结构。通过对FasU活性位点的定点突变👰🏽♀️,并结合分子动力学模拟(MD)分析⛪️,揭示了关键的催化残基,并证实了FasU 的立体专一性来源于结合口袋与 C21 和 C23 羟基之间的疏水排斥作用。这部分工作不仅在II型芳香聚酮骨架的ARO/CYC的种类上实现了大的突破👷🏿♀️,还为未来产生新型ARO/CYC和轴手性芳香聚酮骨架提供了重要思路。
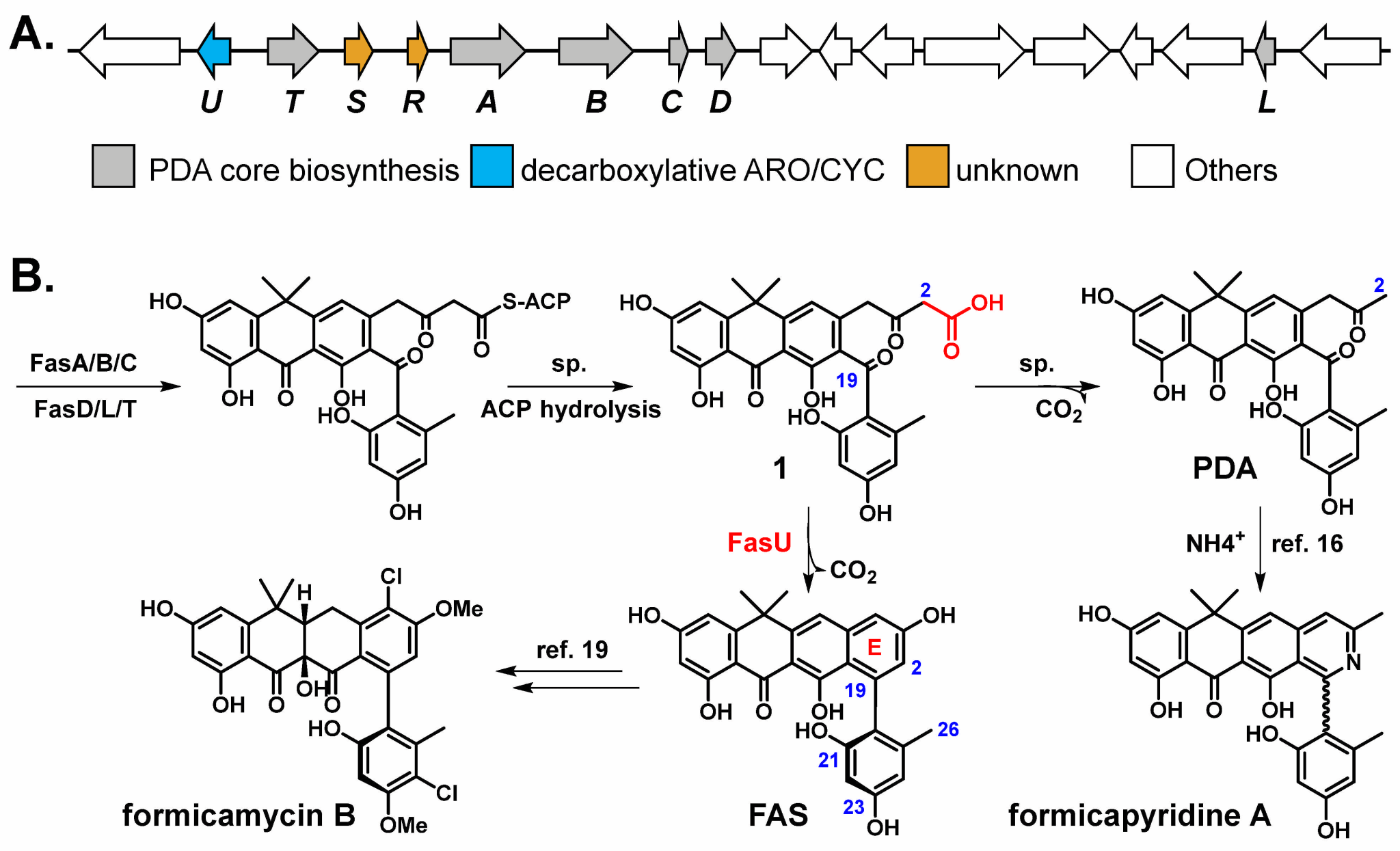
图 2.FAS的生物合成基因簇及生物合成途径。(A) FAS 生物合成基因簇👩🏼✈️。(B) FAS 生物合成途径及其衍生物。
该研究工作受到了国家自然科学基金(32425033,22377074🚶,22107069),上海市优秀学术带头人项目(22XD1421300)以及上海市自然科学基金项目(23ZR1432800)的支持。
论文链接🧙♀️❓:https://pubs.acs.org/doi/10.1021/jacs.4c18376





 交大主页
交大主页